Наследственным раком, или наследственными опухолевыми синдромами, называют онкологические заболевания, которые развиваются из-за передачи из поколения в поколение патогенных генетических мутаций.
На долю наследственного рака приходится около 5–10% всех случаев онкологических заболеваний.
Врачи научились лучше понимать причины возникновения таких опухолей совсем недавно — примерно с середины 1990-х годов. Это стало возможным благодаря развитию технологий геномного анализа.
Чаще всего наследственные опухолевые синдромы связаны с дефектами в генах — супрессорах опухолевого роста. Эти гены также называют антионкогенами.
Антионкогены определяют работу специальных белков-супрессоров, или антионкобелков. Такие белки выполняют очень важную функцию: исправляют ошибки при передаче генетического материала (ДНК), которые иногда возникают в процессе деления клеток.
Но если в генах-супрессорах есть дефект, антионкобелки работают плохо. В результате ошибки при делении клеток накапливаются, что может привести к злокачественному перерождению ткани.
При появлении дефекта в генах-супрессорах антионкобелки перестают работать корректно, что приводит к перерождению здоровой ткани в злокачественную
Часто встречающиеся наследственные опухолевые синдромы:
- наследственный рак молочной железы и яичников,
- наследственный неполипозный рак толстой кишки (синдром Линча),
- семейный аденоматоз толстой кишки,
- наследственный рак щитовидной железы.
Самый частый из них — наследственный рак молочной железы и яичников.
Синдром наследственного рака молочной железы и яичников
По статистике, рак молочной железы занимает 1-е место по частоте встречаемости среди других онкологических заболеваний у женщин.
15 октября — Всемирный день борьбы с раком молочной железы.
Примерно в 10% случаев причина болезни — синдром наследственного рака молочной железы и яичников (hereditary breast and ovarian cancer syndrome, HBOC).
Как следует из названия синдрома, он может приводить не только к раку молочной железы, но и к раку яичников: до 10% случаев рака яичников имеют наследственную природу.
Синдром наследственного рака молочной железы и яичников связан и с другими видами рака, например раком поджелудочной железы. Поэтому синдром опасен не только для женщин. У мужчин он может привести к раку молочной железы, раку простаты и раку поджелудочной железы.
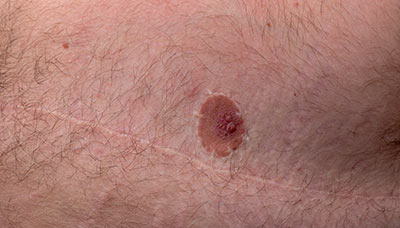
Синдром опасен и для мужчин: он может привести к раку молочной железы (на фото шрам после мастэктомии у мужчины)
Какие генетические мутации приводят к развитию синдрома
Чаще всего синдром развивается из-за мутаций (дефектов) в генах BRCA1 и BRCA2.
Название обоих генов представляет собой аббревиатуру от английских слов breast (BR) — «грудь» и cancer (CA) — «рак», то есть ген рака груди.
О генах BRCA1 и BRCA2 узнали недавно: BRCA1 был открыт в 1994 году, BRCA2 — в 1995-м. Открытие помогло объяснить около трети семейных случаев рака.
В норме BRCA1 и BRCA2 — это гены, позволяющие защитить клетки от злокачественного перерождения.
Ген BRCA1 кодирует белок, который регулирует рост клеток, препятствует их неконтролируемому делению, а также устраняет ошибки при передаче ДНК. Это помогает поддерживать генетическую информацию клетки стабильной. Однако при мутациях BRCA1 кодируемый им белок перестаёт правильно работать. Из-за этого возникает угроза злокачественного перерождения клеток некоторых органов.
Органы, в которых чаще всего развивается рак, при мутациях гена BRCA1:
- молочные железы,
- яичники,
- толстая кишка,
- предстательная железа,
- поджелудочная железа.
Белок-супрессор, за который отвечает ген BRCA2, выполняет примерно такие же функции. При мутации гена BRCA2 может происходить злокачественное перерождение клеток и формирование опухолей некоторых органов.
Органы, в которых чаще всего развивается рак, при мутациях гена BRCA2:
- молочные железы,
- яичники,
- желудок,
- поджелудочная железа,
- предстательная железа,
- кожа.
Реже причиной возникновения синдрома наследственного рака молочной железы и яичников становятся мутации в генах TP53, PTEN, CDH1, ATM, CHEK2, PALB2 и некоторых других.
Какова вероятность унаследовать патогенную мутацию
Синдром наследственного рака молочной железы и яичников передаётся по аутосомно-доминантному типу. Это значит, что если хотя бы у одного из родителей есть патогенная мутация, то с вероятностью 50% ребёнок её унаследует.
Передача генетического дефекта не зависит от пола: патогенную мутацию могут унаследовать как девочки, так и мальчики от любого из родителей.
Чем носительство мутаций отличается от болезни
Носителями мутаций называют здоровых людей, которые унаследовали генетические мутации от одного или обоих родителей.
Как минимум 1% всех людей — носители патогенных мутаций, значительно увеличивающих риск развития злокачественных опухолей.
У носителей мутаций в генах BRCA1 и BRCA2 к 70 годам риск развития рака молочной железы возрастает на 65% (заболеет около 6 человек из 10 носителей мутаций), а риск развития рака яичников — на 39% (заболеет около 4 из 10 носителей).
Кроме того, у них повышается риск развития других видов рака, включая рак предстательной, поджелудочной железы, а также рак молочной железы у мужчин.
Оценка риска наследственного рака молочной железы и яичников
Если в семье пациента или у него самого уже были случаи рака молочной железы или рака яичников, риск того, что причиной болезни выступает наследственный синдром, значительно возрастает.
Ситуации повышенного риска наследственного рака:
- у близкого родственника диагностировали синдром наследственного рака молочной железы и яичников;
- у родственников первой линии родства (мать, сестра, дочь) выявили 2 случая рака молочной железы, причём хотя бы в одном из случаев пациентка была моложе 50 лет;
- у родственников первой или второй линии родства в любом возрасте выявили не менее 3 случаев рака молочной железы;
- у родственников первой или второй линии родства в любом возрасте выявили одновременно и рак молочной железы, и рак яичников;
- у родственников первой линии родства выявили рак обеих молочных желёз;
- у родственников первой или второй линии родства выявили не менее 2 случаев рака яичников;
- у родственника мужского пола выявили рак молочной железы;
- принадлежность к евреям ашкенази.

Среди евреев ашкенази высоко распространён синдром наследственного рака молочной железы и яичников
В случае если у женщины ранее уже был выявлен рак молочной железы или рак яичников, а также если такие заболевания были диагностированы у близких родственников, целесообразно пройти генетическое исследование, чтобы узнать, унаследовала ли она патогенные мутации.
Классический метод генетического исследования — ПЦР (полимеразная цепная реакция). ПЦР-тест позволяет проанализировать 8 наиболее распространённых мутаций, связанных с риском развития рака молочной железы. Такой тест доступен по цене, а его результат может быть получен достаточно быстро. Поэтому ПЦР-анализ рекомендуется пациенткам из группы риска — с личным или семейным анамнезом рака молочной железы или рака яичников.
Более современный и информативный метод исследования — NGS (next generation sequencing — «секвенирование нового поколения»). NGS-тест считают золотым стандартом для диагностики предрасположенности к раку: в отличие от ПЦР-тестов, он прочитывает анализируемые гены целиком. Именно непрерывное, а не выборочное считывание генов позволяет выявить все имеющиеся патогенные мутации.
В некоторых случаях синдром наследственного рака молочной железы и яичников связан с мутациями не только в генах BRCA1 и BRCA2, но и в других генах, например CHEK2 и ATM. Если у близких родственников пациента были диагностированы злокачественные новообразования молочной железы или яичников, может быть полезно проверить носительство патогенных мутаций не только в генах BRCA1 и BRCA2, но и в других генах.
Результаты исследования помогут врачу оценить риск развития онкологического заболевания у пациента и разработать эффективную стратегию профилактики.
Диагностика рака молочной железы и рака яичников
Для диагностики рака молочной железы или рака яичников любого типа (как наследственного, так и ненаследственного) после консультации у врача (гинеколога, маммолога, онколога) и осмотра проводятся инструментальные и лабораторные исследования, которые помогают уточнить диагноз.
Лабораторные исследования в диагностике рака молочной железы
В рамках лабораторной диагностики рака молочной железы врач может назначить общий и биохимический анализы крови, общий анализ мочи, коагулограмму, а также биопсию опухоли с проведением цитологического, гистологического, иммуногистохимического исследования (определение экспрессии рецепторов к эстрогенам (ER) и прогестерону (PR), исследование белка к рецепторам HER2, индекса пролиферативной активности экспрессии Ki67).
При гормонозависимом раке молочной железы у пациентки до 60 лет с отсутствием менструаций — назначается также определение уровня фолликулостимулирующего гормона (ФСГ) и общего эстрадиола.
При подозрении на синдром наследственного рака молочной железы и яичников возможно генетическое исследование на наличие мутаций в генах BRCA1 и BRCA2.
При спорном результате иммуногистохимического исследования на HER2/Neu проводят дополнительный анализ гистологического материала методом гибридизации in situ (FISH).
При необходимости может назначаться анализ на белок PD-L1, выполняемый иммуногистохимическим методом, а также тест на определение мутаций в гене PIK3CA.
Инструментальные исследования в диагностике рака молочной железы
Распространённые инструментальные исследования:
- билатеральная (двухсторонняя) маммография;
- УЗИ молочных желёз и регионарных лимфатических узлов;
- при наличии показаний (возраст до 30 лет, выявленные мутации в генах BRCA1, BRCA2 и др.) — МРТ молочных желёз;
- УЗИ органов брюшной полости, забрюшинного пространства, малого таза;
- при сомнительных результатах УЗИ органов брюшной полости — КТ или МРТ органов брюшной полости с внутривенным контрастированием;
- КТ или рентгенография органов грудной клетки;
- при подозрении на распространение метастазов — сцинтиграфия костей всего тела.
На этапе диагностики рака молочной железы или рака яичников также целесообразно оценить состояние сердца пациента методом ЭКГ.

Маммографический снимок молочной железы
Лабораторные исследования в диагностике рака яичников
В рамках лабораторной диагностики рака яичников врач может назначить общий и биохимический анализы крови, общий анализ мочи, коагулограмму, а также определение уровня в крови онкомаркеров СА 125, HE4, индекса ROMA.
При подозрении на муцинозную карциному также могут быть назначены анализы на онкомаркер CA 19-9 и РЭА.
При подозрении на синдром наследственного рака молочной железы и яичников назначают генетическое исследование на наличие мутаций в генах BRCA1 и BRCA2.
При подозрении на рак яичников целесообразно провести цитологическое исследование мазков шейки матки и цервикального канала, а также аспирата из полости матки.
Чтобы уточнить стадию рака яичников, пациенткам могут порекомендовать цитологическое исследование аспиратов/пунктатов/смывов с брюшины, экссудата плевральных или брюшной полостей.
Инструментальные исследования в диагностике рака яичников
В рамках комплексной диагностики рака яичников врач может назначить инструментальные исследования.
Эзофагогастродуоденоскопия (ЭГДС) применяется для дифференциальной диагностики опухоли желудочно-кишечного тракта и опухоли яичников: при злокачественном новообразовании желудка опухоль яичников может оказаться вторичной (метастазы) по отношению к основной опухоли.
Колоноскопия проводится для дифференциальной диагностики с опухолями кишечника.
Компьютерную томографию (КТ) органов грудной клетки, брюшной полости и забрюшинного пространства, почек назначают, чтобы определить, насколько распространилась опухоль, и спланировать лечение.
Магнитно-резонансная томография (МРТ) органов малого таза проводится с той же целью, что и КТ.
Рентгенография органов грудной клетки выполняется, если нет возможности выполнить КТ органов грудной клетки.
Ультразвуковое исследование (УЗИ) лимфатических узлов шейно-надключичной, подмышечной, паховой области назначают, если нет возможности выполнить КТ/МРТ/ПЭТ-КТ.
УЗИ молочных желёз (рекомендуется пациенткам до 40 лет) и маммография (рекомендуется пациенткам старше 40 лет) проводятся, чтобы исключить метастатическое распространение рака яичников или первичное одновременное поражение яичников и молочных желёз.
Диагностическая лапароскопия (малоинвазивная операция, при которой вместо одного большого разреза брюшной полости выполняют несколько небольших) может потребоваться для уточнения диагноза и планирования лечения.
Полученный во время диагностической операции материал направляют на исследование: это помогает оценить строение и степень злокачественности опухоли и спланировать лечение.
Факторы, которые могут указывать на наследственный рак
Когда врач может заподозрить наследственный рак:
- если рак молочной железы выявлен у пациентки моложе 50 лет;
- если рак молочной железы выявлен в любом возрасте у пациентки, родственникам которой диагностировали рак молочной железы в возрасте до 50 лет;
- если рак молочной железы выявлен у пациентки во второй раз или чаще, причём первый случай болезни выявлен, когда пациентка была моложе 50 лет;
- если рак молочной железы выявлен в любом возрасте у пациентки, родственникам которой диагностировали метастатический рак простаты, рак яичников или рак поджелудочной железы;
- если выявили трижды негативный рак молочной железы (одна из наиболее агрессивных разновидностей рака молочной железы) у человека в возрасте до 60 лет;
- если рак молочной железы выявили у мужчины.
Лечение наследственного рака молочной железы и яичников
Выявленную опухоль молочной железы или яичников удаляют, а затем проводят лучевую терапию или химиотерапию.
Виды операций при раке молочной железы:
- органосохраняющие операции (секторальная резекция с биопсией сигнальных лимфатических узлов) — при новообразовании небольшого размера и неагрессивной природы;
- операции по удалению всей ткани молочной железы и подкожно-жирового слоя (мастэктомия), по показаниям также удаляют некоторые лимфатические узлы (лимфаденэктомия) — при новообразованиях большого размера или неблагоприятном прогнозе болезни (трижды негативный рак молочной железы и другие агрессивные виды опухолей, поражение подмышечных лимфатических узлов).
Виды операций при раке яичников:
- органосохраняющие операции, например удаление только одного яичника с резекцией второго яичника, удаление большого сальника, лимфатических узлов тазовой и поясничной областей — у молодых пациенток, которые хотят сохранить фертильность, при серозной карциноме низкой степени злокачественности, эндометриоидной или муцинозной карциноме IA и IC1 стадий, если установлено, что рак яичников ненаследственного характера;
- удаление обоих яичников, маточных труб, матки, лимфатических узлов — в остальных случаях.
Назначение химиотерапии и лучевой терапии проводится в зависимости от стадии болезни, молекулярно-биологического подтипа опухоли, наличия или отсутствия метастазов.
А если подтверждён наследственный характер опухоли, применяют таргетные препараты, которые воздействуют на конкретные гены-мишени.
К какому врачу обращаться при семейном РМЖ/РЯ
Диагностикой и лечением синдрома наследственного рака молочной железы и яичников занимаются гинеколог, маммолог, онколог.
Чтобы оценить риск развития наследственного рака у здорового носителя патогенных мутаций, целесообразно обратиться за консультацией к врачу-генетику.
Прогноз семейного РМЖ/РЯ
Прогноз наследственного рака молочной железы и яичников сильно зависит от своевременности генетической диагностики и подбора подходящей терапии. Новые методы лечения наследственного рака (платиносодержащие препараты при раке яичников, таргетные препараты) позволяют существенно отсрочить рецидив болезни и увеличить продолжительность жизни пациентов.
Профилактика наследственного рака молочной железы и яичников
Для профилактики развития наследственного рака важно своевременно выявить носительство патогенных мутаций.
Если у человека обнаружили мутации в генах BRCA1 и BRCA2, ему следует сообщить об этом близким родственникам и предложить пройти генетическое тестирование.
Важно проводить самообследование молочных желёз. Для этого ежемесячно (на 5–6-й день менструального цикла, а в период менопаузы — в один и тот же день месяца) нужно осматривать грудь, стоя у зеркала с поднятыми руками, а также ощупывать её в положении стоя и лёжа на спине. Во время самообследования в груди не должны обнаруживаться никакие уплотнения, отёки, не должно быть покраснений, трещин или других изменений на коже груди и на сосках. Из сосков не должно быть выделений.
Также целесообразно обсудить с врачом-онкологом, какие обследования стоит пройти в рамках скрининга рака молочной железы и рака яичников. Врач может порекомендовать сделать маммографию, МРТ молочных желёз, УЗИ малого таза, сдать анализ крови на онкомаркеры и др. Список анализов и обследований подбирается вместе с врачом в индивидуальном порядке. Такой скрининг полезно проходить не реже одного раза в год.
Что делать здоровым носителям патогенных мутаций
Радикальная мера профилактики для здоровых носителей патогенных мутаций — это превентивная мастэктомия или овариэктомия, то есть удаление здоровых молочных желёз или яичников до того, как произошло злокачественное изменение клеток этих органов.
О превентивной мастэктомии многие люди узнали в 2013 году благодаря американской актрисе Анджелине Джоли. Ей пришлось сделать такую операцию из-за высокого риска развития наследственного рака молочной железы: от этой болезни умерли её мать и бабушка, а у самой актрисы обнаружили мутацию в гене BRCA1.
В целом, превентивные операции можно считать наиболее эффективным методом профилактики наследственных опухолей. Однако есть данные, что в редких случаях даже после таких операций у пациентов всё равно развивались опухоли: рак молочной железы из клеток, оставшихся после удаления молочных желёз, или перитонеальная карцинома после удаления яичников.
Профилактическое удаление здоровых органов — непростое решение. Кроме того, в России проведение таких операций сопряжено с рядом трудностей, в том числе негативным отношением медицинского сообщества к удалению здоровых органов, а также неурегулированной законодательной базой.